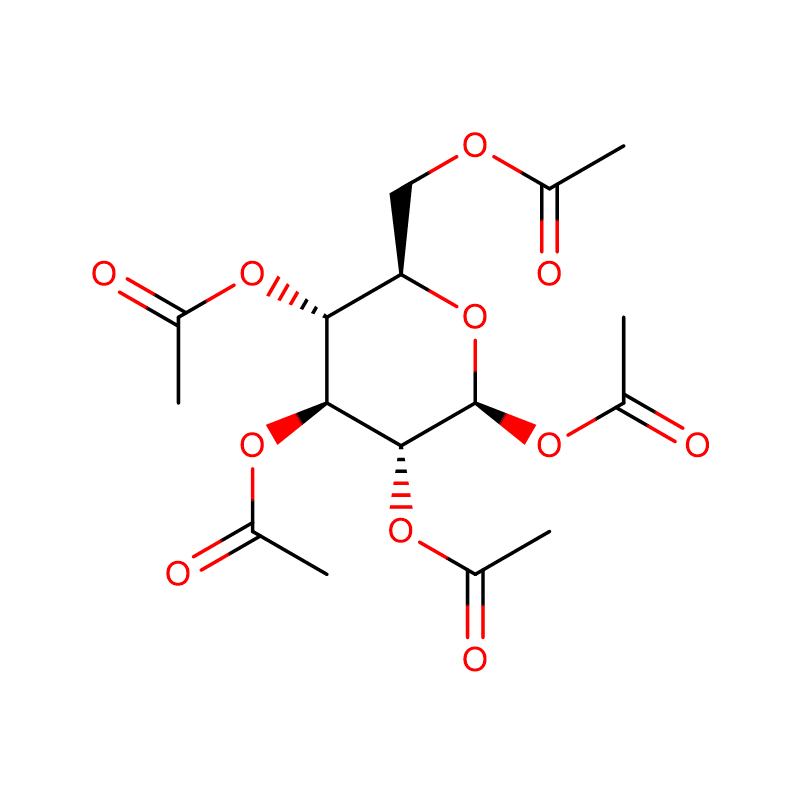
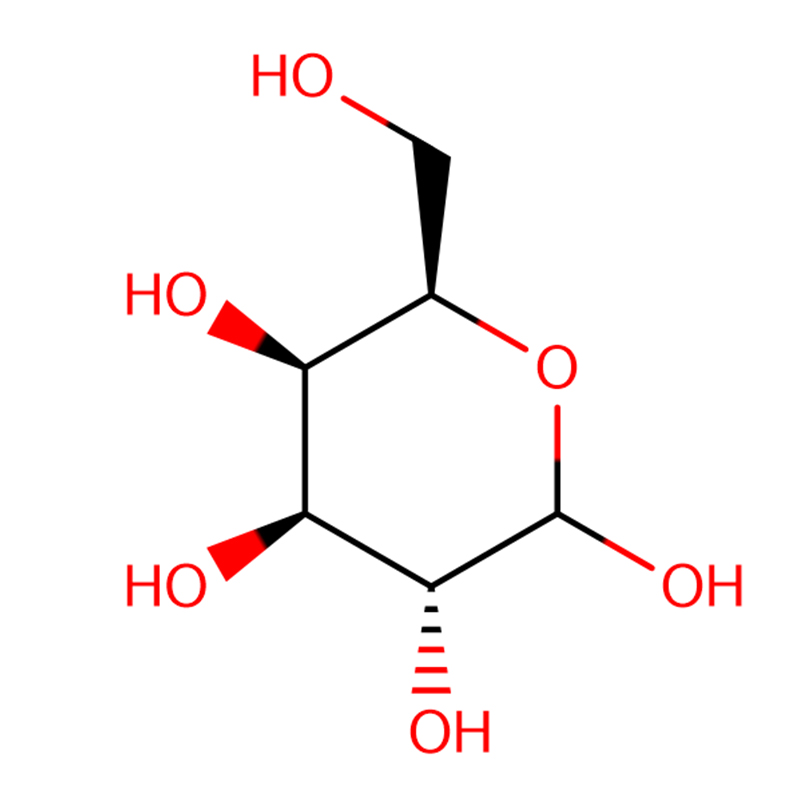
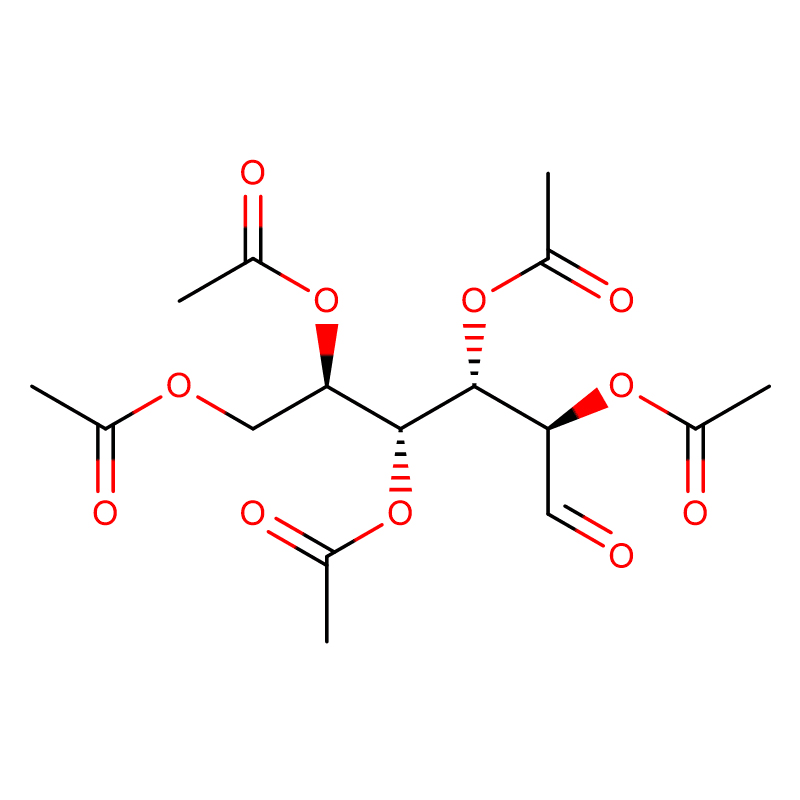
4-НІТРАФЕНІЛ-АЛЬФА-D-МАНАПІРАНАЗІД CAS:10357-27-4 Бэзавы парашок 98%
| Нумар па каталогу | XD90011 |
| Назва прадукту | 4-Нитрофенил-альфа-D-маннопиранозид |
| CAS | 10357-27-4 |
| Малекулярная формула | C12H15NO8 |
| Малекулярная маса | 30301.25 |
| Дэталі захоўвання | -2да -8°C |
| Гарманізаваны тарыфны кодэкс | 29400000 |
Спецыфікацыя прадукту
| вада | <5% Карл Фішэ |
| Растваральнасць | 1% у DMF празрысты і бескаляровы |
| Чысціня | Свабодны 4-нітрафенол <200 частак на мільён |
| ВЭЖХ | >98% |
| Знешні выгляд | Брудна-белы парашок |
Механістычнае разуменне Ca2 + -залежнай сям'і альфа-маннозидаз ў кішачніку чалавека сімбіёнта.
Бактэрыі тоўстай кішкі, прыкладам якіх з'яўляецца Bacteroides thetaiotaomicron, гуляюць ключавую ролю ў падтрыманні здароўя чалавека, выкарыстоўваючы вялікія сем'і глікозід-гідралаз (GH) для выкарыстання харчовых поліцукрыдаў і гліканаў гаспадара ў якасці пажыўных рэчываў.Прыкладам такога пашырэння сямейства GH з'яўляюцца гліказідазы 23 сямейства GH92, якія кадуюцца геномам B. thetaiotaomicron.Тут мы паказваем, што гэта альфа-манназідазы, якія дзейнічаюць з дапамогай адзінага механізму выцяснення для выкарыстання N-гліканаў гаспадара.Трохмерная структура дзвюх манназідаз GH92 вызначае сямейства двухдаменных бялкоў, у якіх каталітычны цэнтр размешчаны на мяжы даменаў, забяспечваючы кіслату (глутамат) і аснову (аспартат) спрыяючым гідролізу ў Ca(2+)- залежны лад.Трохмерныя структуры GH92 у комплексе з інгібітарамі даюць зразумець спецыфіку, механізм і канфармацыйны маршрут каталізу.Ca(2+) адыгрывае ключавую каталітычную ролю, дапамагаючы сказіць манназід ад яго асноўнага стану (4)C(1) канфармацыі крэсла да пераходнага стану. (Бібліяграфія: Нац.хім.біял.6, 125-32, (2010)
Франтальная аффинная храматаграфія гликоаспарагинов овальбумина на калонцы канканавалина А-сефарозы.Колькаснае даследаванне спецыфічнасці звязвання лектина.
Узаемадзеянне сефарозы 4В-імабілізаванага канканаваліна А (ConA) з 10 глікааспарагінамі, атрыманымі з овальбумина, даследавалі колькасна з дапамогай франтальнай аффинной храматаграфіі.У гэтым метадзе раствор вугляводаў бесперапынна наносіцца на калонку ConA-Sepharose і запаволенне фронту элюіравання вымяраецца як параметр сілы ўзаемадзеяння.Канстанта дысацыяцыі (Kd) для кожнага сахарида можа быць вызначана з ConA.Аналіз звязвання p-нитрофенил-альфа,D-маннозида паказаў, што звязваюць ўласцівасці ConA істотна не змяняюцца пасля імабілізацыі на сефарозе 4B.Кожны з глікааспарагінаў авальбуміна быў пазначаны трыціем метадам аднаўленчага метилирования для аналізу.Параўнанне атрыманых значэнняў Kd паказала, што звязванне ConA значна вар'іруецца з вельмі нязначнымі структурнымі адрозненнямі гликозильной ланцуга.Вынікі паказваюць, што ConA распазнае спецыфічную структуру гліказільнай ланцуга Man alpha 1-6 (Man alpha 1-3) Man, у якой хаця б адна гідраксільная група ў становішчы C-3 маннозы, звязанай з C-6, павінна быць свабоднай.