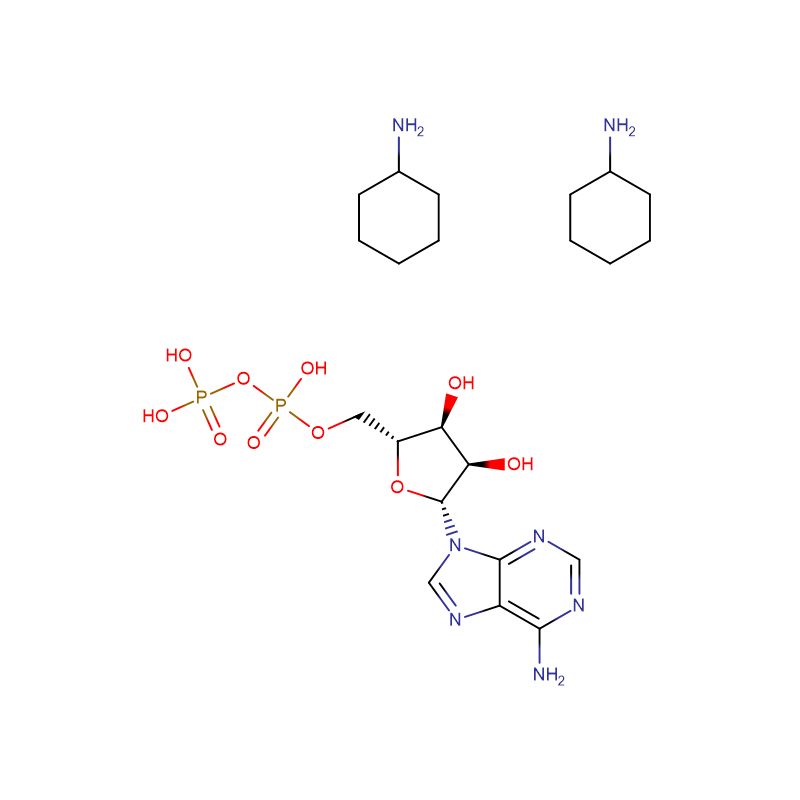
адэназін 5'-дыфасфат ды (монацыклагексіламоній Cas: 102029-87-8 99% Белы парашок
| Нумар па каталогу | XD90159 |
| Назва прадукту | адэназін 5'-дыфасфат ды (монацыклагексіламоній |
| CAS | 102029-87-8 |
| Малекулярная формула | C10H15N5O10P2·2C6H13N |
| Малекулярная маса | 625,55 |
| Дэталі захоўвання | ад 2 да 8 °C |
| Гарманізаваны тарыфны кодэкс |
Спецыфікацыя прадукту
| Знешні выгляд | Белы парашок |
| Ассаy | 99% |
1. Даследаваць, ці можа адэназін, атрыманы з адэназіндыфасфату (АДФ), інгібіраваць агрэгацыю трамбацытаў, асабліва ў прысутнасці антаганіста P2Y₁₂, калі ўздзеянне АДФ на рэцэптар P2Y₁₂ будзе прадухілена. Агрэгацыя трамбацытаў вымяралася ў адказ на актыватар рэцэптара трамбіну пептыда шляхам падліку трамбацытаў у багатай трамбацытамі плазме (PRP) і суцэльнай крыві ў прысутнасці АДФ і антаганістаў P2Y₁₂ кангрэлора, актыўнага метабаліту прасугрэла і тикагрелора.У прысутнасці антаганіста P2Y₁₂ папярэдняя інкубацыя PRP з АДФ інгібіравала агрэгацыю;гэты эфект быў адменены аденозиндезаминазой.Ніякага інгібіравання агрэгацыі не адбылося ў суцэльнай крыві, за выключэннем выпадкаў, калі дыпірыдамол быў дададзены для інгібіравання паглынання адэназіну эрытрацытамі.Эфекты АДФ у PRP і суцэльнай крыві былі прайграныя з выкарыстаннем адэназіну і былі непасрэдна звязаны са зменамі ў цАМФ (ацэненым па фасфараляванню фасфапратэінаў, стымулюемым судзінапашыральным сродкам).Усе вынікі былі аднолькавымі незалежна ад выкарыстоўванага агоніста P2Y₁₂. АДФ інгібіруе агрэгацыю трамбацытаў у прысутнасці антаганіста P2Y12 праз ператварэнне ў адэназін.Інгібіраванне адбываецца ў PRP, але не ў суцэльнай крыві, за выключэннем выпадкаў, калі інгібіруецца паглынанне адэназіну.Ні адзін з вывучаных антаганістаў P2Y₁₂ не паўтарыў эфекты дыпірыдамола ў праведзеных эксперыментах.
2. АДФ лічыцца слабым агоністом трамбацытаў з-за абмежаваных рэакцый агрэгацыі, якія ён індукуе in vitro пры фізіялагічных канцэнтрацыях пазаклеткавага Ca(2+) [(Ca(2+) )(o)].Зніжэнне [Ca(2+)](o) парадаксальным чынам узмацняе выкліканую АДФ агрэгацыю, эфект, які тлумачыцца ўзмоцненай выпрацоўкай тромбоксана А(2).Гэта даследаванне вывучала ролю эктануклеатыдаз у [Ca(2+)](o) -залежнасці актывацыі трамбацытаў.Зніжэнне [Ca(2+)](o) з миллимолярных да микромолярных узроўняў пераўтварыла выкліканую АДФ (10 мкмоль/л) агрэгацыю трамбацытаў з мінучай у ўстойлівую рэакцыю як у багатай трамбацытамі плазме, так і ў прамытай завісі.Блакаванне выпрацоўкі тромбоксана А(2) аспірынам не аказвала ўплыву на гэтую [Ca(2+)](o) -залежнасць.Прадухіленне дэградацыі АДФ скасавала адрозненні паміж нізкім і фізіялагічным [Ca(2+)](o), што прывяло да трывалай і ўстойлівай агрэгацыі ў абодвух умовах.Вымярэнні пазаклеткавай АДФ паказалі зніжэнне дэградацыі як у плазме, так і ў фізіялагічным растворы, які змяшчае апіразу, у мікрамолярным у параўнанні з мілімалярным [Ca(2+)](o).Як паведамлялася раней, выпрацоўка трамбаксану A(2) узмацнялася пры нізкім узроўні [Ca(2+)](o), аднак гэта не залежала ад актыўнасці эктануклеатыдазы(.) Антаганісты рэцэптараў P2Y кангрелор і MRS2179 прадэманстравалі неабходнасць рэцэптараў P2Y(12). для ўстойлівай ADP-выкліканай агрэгацыі, з нязначнай роляй для P2Y(1) .У заключэнне, Са(2+) -залежная эктануклеатыдазная актыўнасць з'яўляецца асноўным фактарам, які вызначае ступень агрэгацыі трамбацытаў да АДФ, і яе неабходна кантраляваць у даследаваннях актывацыі рэцэптара P2Y.