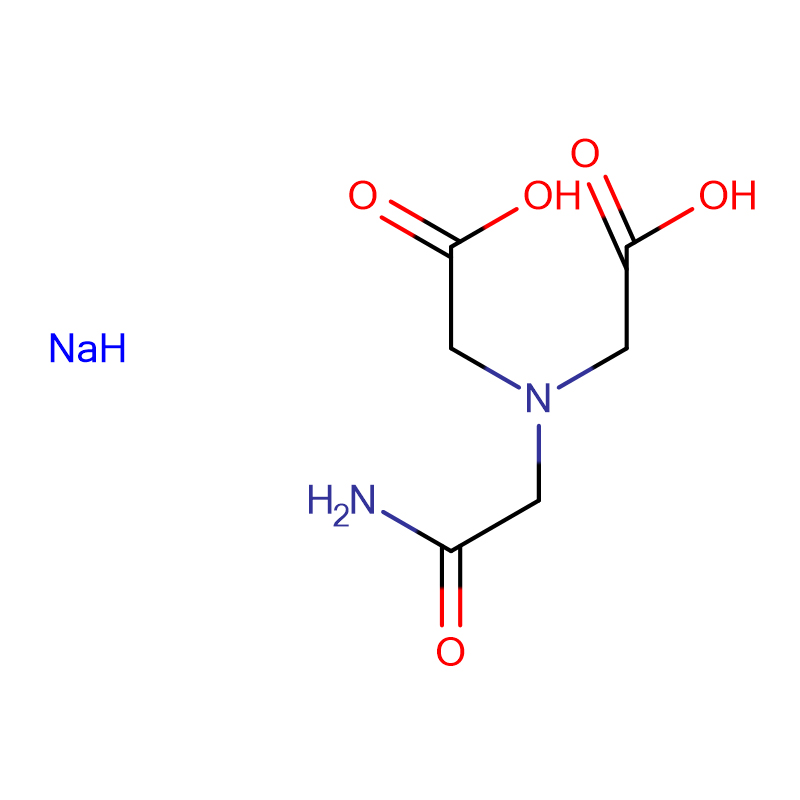
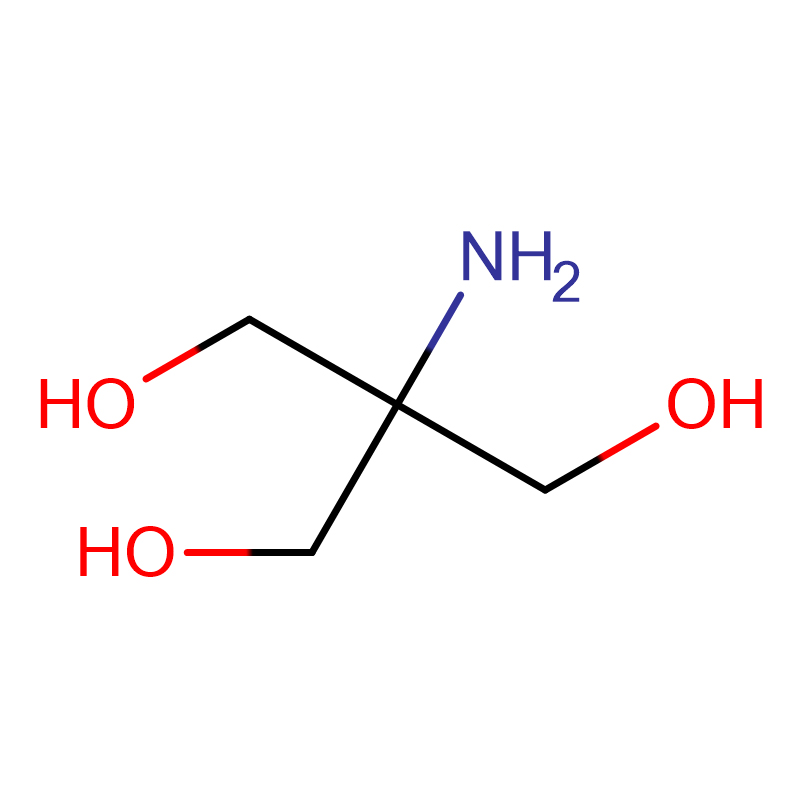
Двунатрыевая соль ADA Cas:41689-31-0 N- (2- аміна- 2- оксаэтыл)- N- (карбаксіметыл) гліцынадынатрыевая соль Белы крышталічны парашок 98%
| Нумар па каталогу | XD90092 |
| Назва прадукту | АДА Двунатрыевая соль |
| CAS | 41689-31-0 |
| Малекулярная формула | H2NCOCH2N(CH2CO2Na)2 |
| Малекулярная маса | 234.12 |
| Дэталі захоўвання | Эмбіент |
| Гарманізаваны тарыфны кодэкс | 292419009 |
Спецыфікацыя прадукту
| Знешні выгляд | Белы крышталічны парашок |
| Ассаy | >98,0% |
| Тэмп. захоўвання | Захоўваць у RT |
Буфер - гэта раствор, які можа супрацьстаяць змене pH пры даданні невялікай колькасці кіслаты або шчолачы і вады.Буферная сістэма pH гуляе важную ролю ў падтрыманні нармальнага значэння pH арганізмаў і нармальнай фізіялагічнай асяроддзя.Большасць клетак можа працаваць толькі ў вельмі вузкім дыяпазоне pH.Ён павінен мець буферную сістэму, каб супрацьстаяць зменам pH, якія адбываюцца падчас метабалізму.У арганізме існуюць тры асноўныя буферныя сістэмы рн: бялковыя і бікарбанатныя буферныя сістэмы.Колькасць кожнай буфернай сістэмы адрозніваецца ў розных тыпах клетак і органаў.
Буфернае дзеянне на кіслату буфернага раствора, які складаецца з слабой кіслаты НА і яе солі NaA, абумоўлена наяўнасцю ў растворы дастатковай колькасці шчолачы А-.Калі ў гэты раствор дадаецца пэўная колькасць моцнай кіслаты, іёны Н па сутнасці спажываюцца іёнамі А:
Такім чынам, значэнне pH раствора амаль не змяняецца;калі дадаецца пэўная колькасць моцнай асновы, слабая кіслата HA ў растворы спажывае іёны OH- і перашкаджае змене pH.
Дадайце невялікую колькасць моцнай кіслаты або моцнай асновы ў буферны раствор, значэнне pH раствора не моцна зменіцца, але калі дадаць колькасць кіслаты або шчолачы, буферны раствор страціць свой буферны эфект.Гэта паказвае, што яго буферная ёмістасць мае пэўны мяжа.
Буферная здольнасць буфернага раствора звязана з канцэнтрацыяй кампанентаў, якія ўваходзяць у склад буфернага раствора.Буферны раствор, які складаецца з 0,1 моль·л-1HAc і 0,1 моль·л-1NaAc, мае большую буферную здольнасць, чым буферны раствор з 0,01 моль·л-1HAc і 0,01 моль·л-1NaAc.Гэта можна пацвердзіць разлікамі.Аднак канцэнтрацыя кампанентаў буфернага раствора не павінна быць занадта вялікай, у адваротным выпадку нельга не ўлічваць ўзаемадзеянне паміж іёнамі.